Images of Wikipedia:管理者伝言板/拡張承認の申請

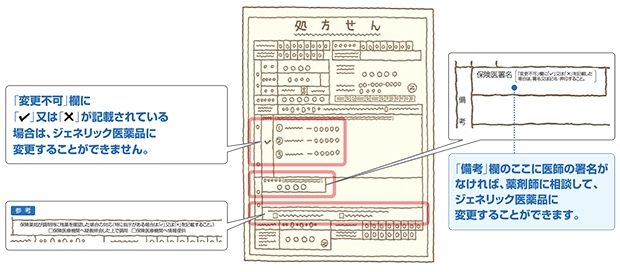
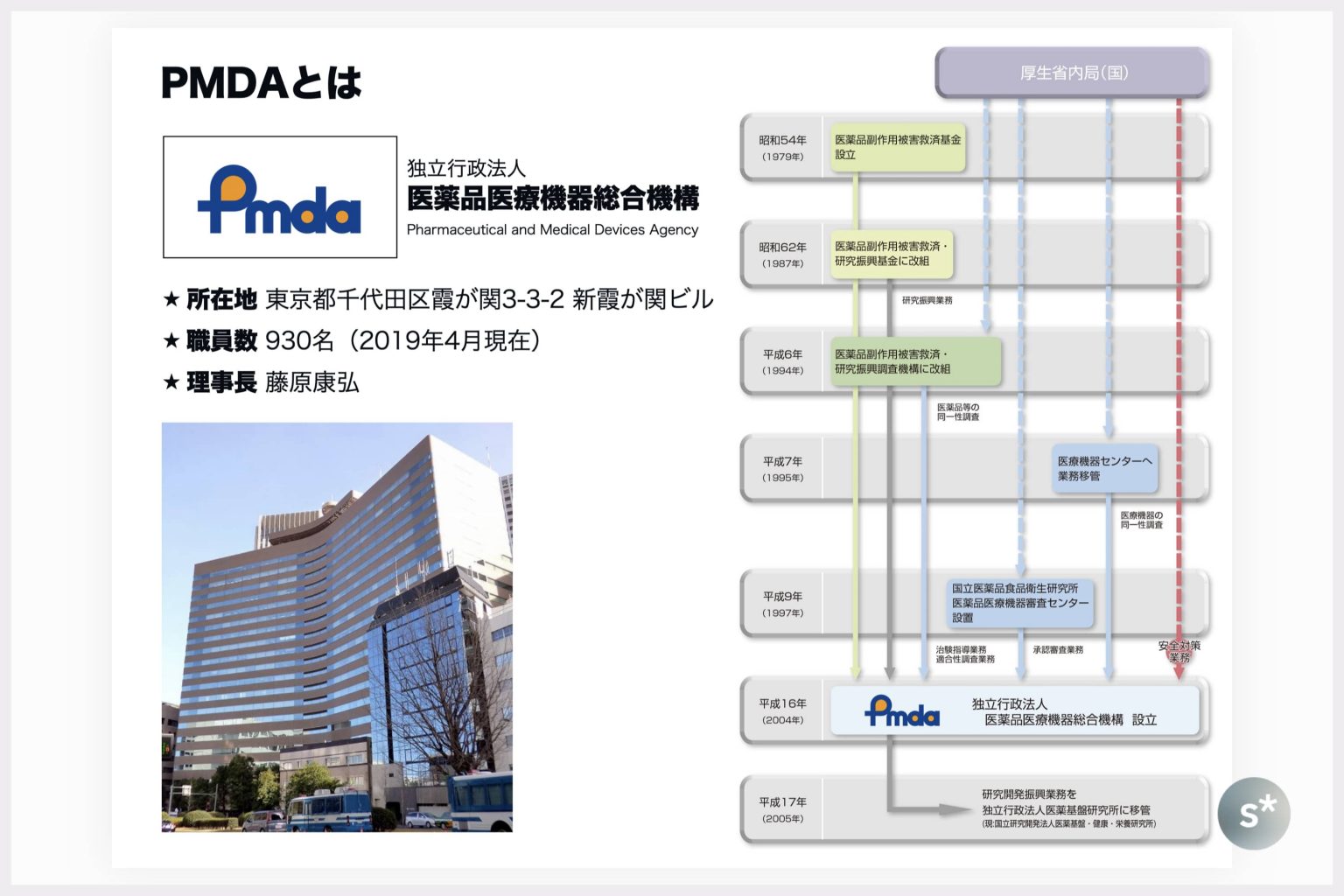
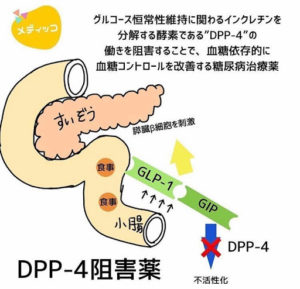
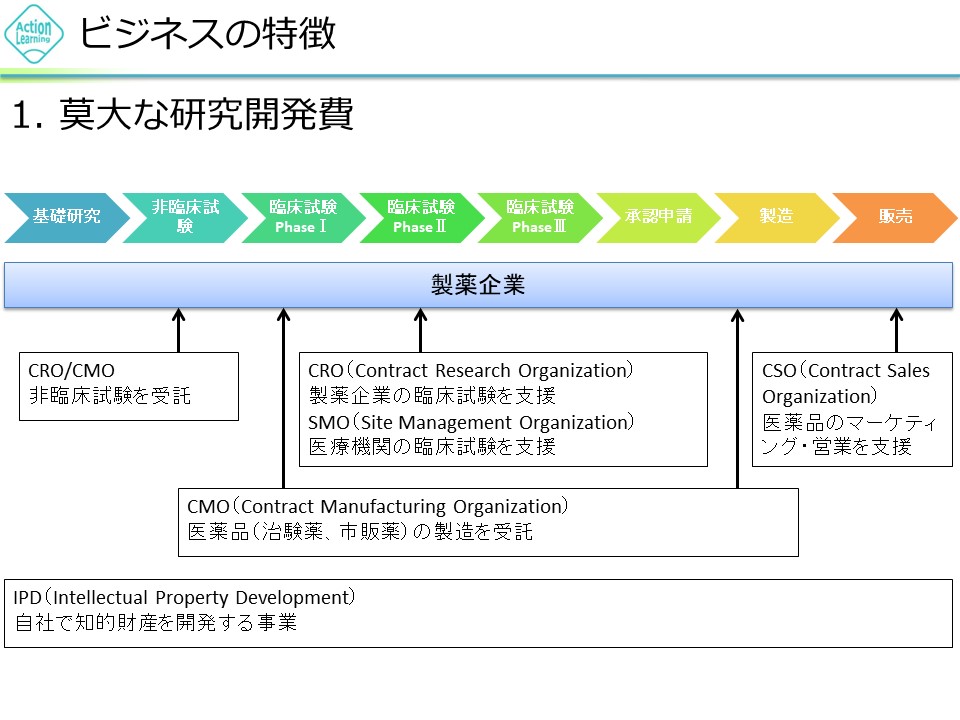
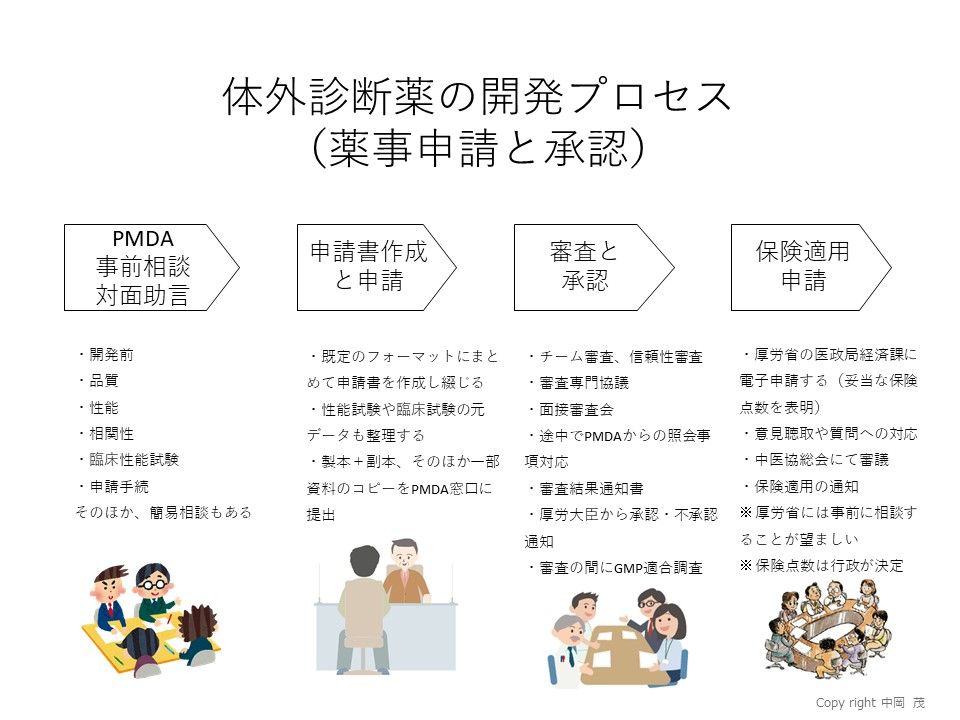
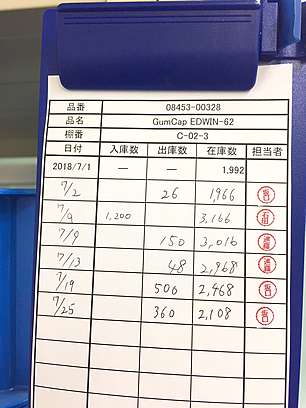
4551 - 鳥居薬品(株) 新薬の申請から承認までにかかる期間。(画像参照) 優先品目に関しては別にある。今回は通常品目。 PMDA 独立行政法人 医療品医療器総合機構のHPより。 申請から承認、約1年くらいなんでしょうかね!?間違ってたらごめんなさい!

【【がん】2020年に日米欧で承認された主な新薬】(★は先駆け審査指定制度(日)、ブレークスルーセラピー(米)、PRIME指定(欧)の対象)(―は未開発または開発段階不明)(製品名(一般名)/社名/適応/承認年/開発段階(日)/(米)/(欧)): 「Polivy」(polatuzumab vedotin)/ロシュ/びまん性大細胞型B細胞リンパ腫/申請/19★/20★ |「ニュベクオ」(ダロルタミド)/バイエル/去勢抵抗性前立腺がん/20/19/20 |「Ayvakit/Ayvakyt」(avapritinib)/米ブループリント/PDGFRA Exon 18変異型消化管間質腫瘍/―/20★/20 |「Tazverik」(tazemetostat)/米エピザイム/類上皮肉腫/濾胞性リンパ腫/申請/20★/― |「ベレキシブル」(チラブルチニブ)/小野薬品/中枢神経系原発リンパ腫/原発性マクロブリン血症およびリンパ形質細胞リンパ腫/20/―/― |「サークリサ」(イサツキシマブ)/サノフィ/多発性骨髄腫/20/20/20 |「カボメティクス/Cometriq」(カボザンチニブ)/米エクセリシス/武田薬品/仏イプセン/腎細胞がん/肝細胞がん/20/12★/14 |「エンハーツ」(トラスツズマブ デルクステカン)/第一三共/HER2陽性乳がん/HER2陽性胃がん/20★/19★/21 |「Trodelvy」(sacituzumab govitecan)/ギリアド/トリプルネガティブ乳がん/―/20★/― |「テプミトコ」(テポチニブ)/独メルク/MET遺伝子変異陽性非小細胞肺がん/20★/申請/申請 |「ステボロニン」(ボロファラン(10B))/ステラファーマ/頭頸部がん/20★/―/― |オニバイド/仏セルヴィエ/仏イプセン/膵がん/20/15/16 イリノテカン |「Pemazyre」/米インサイト/FGFR2融合遺伝子/申請/20★/申請 pemigatinib/陽性胆管がん/ 「Koselugo」(selumetinib)/アストラゼネカ/米メルク/小児の神経線維腫症1型/P1/20★/申請 |「Jelmyto」(mitomycin)/米ユーロジェン/低悪性度の上部尿路上皮がん/―/20★/― |「Tukysa」(tucatinib)/米シーゲン/HER2陽性乳がん/―/20★/申請 |「Retevmo」(selpercatinib)/イーライリリー/RET融合遺伝子陽性非小細胞肺がん/RET遺伝子変異型甲状腺がん/開発 後期/20★/申請 |「カルケンス」(アカラブルチニブ)/アストラゼネカ/慢性リンパ性白血病/21/17★/20 |「Qinlock」(ripretinib)/米デシフェラ/消化管間質腫瘍/―/20★/申請

2160 - (株)ジーエヌアイグループ 中国の早期承認プロセスには下記5種類が有り、F351の本道である肝線維症は③の画期的治療薬に指定済、肝硬変は②の迅速承認にて会社はCDEに相談する方針と発表済だが別のプロセス。 で前回のIRは「まもなく笑」に関しての、三相開始の件で迅速承認申請とはもちろん別物、ただ画期的治療薬自体が早期承認プロセスの1つで有るとこには変わりはない。 因みに中国の画期的治療薬制度のモデルになってる米FDAの1例を上げると、先月米FDAより画期的治療薬に指定されたアルツハイマー治療薬(アミロイドβ除去薬)であるイーライリリーの新薬候補は年内に迅速承認制度にて申請を行う予定との事、約半年で申請を行える。 仮にF351が迅速承認制度で承認を得たとしても最長3年治験を終えデータを提出する事にはなる、3年治験をする予定だから早期承認が無くなったと結論付けるのは尚早かと。